您是否听说过临床试验?
您是否参加过临床试验?
临床试验是如何产生的?
下面简单地和大家介绍一下临床试验的著名历史事件,感兴趣的小伙伴可自行查阅相关资料。

一、临床试验的起源
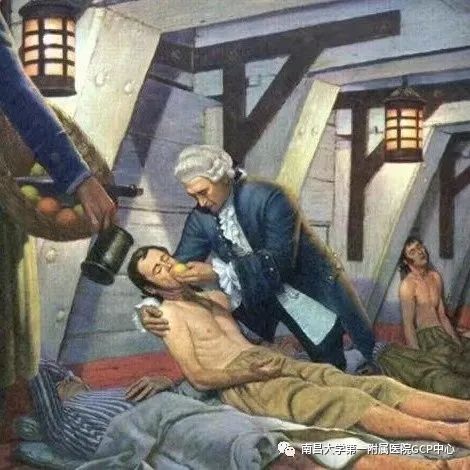
1747年5月20日,苏格兰海军军医詹姆斯·林德(James Lind)在索尔兹伯里号上选了12名坏血病船员,将他们分为6组,每组2人,分别给予苹果酒、稀硫酸、醋、海水、香料、大蒜、芥子混合物以及橘子、柠檬等6种不同的方法进行治疗。6天后,2名接受橘子和柠檬治疗的海员1名已经可以正常工作,而另1名也已经恢复到可以照顾其他患病海员。1753年,James以“A treatise of the scurvy”为报告,报道了此项试验结果,尽管当时无法知道橘子和柠檬的治疗原理(后来研究发现含有 Vitamin C),但是,鉴于该试验记录完整,具有设计对照、控制、前瞻性的特点,因此,这次著名的“坏血病临床试验”被认为开创了临床试验的先河。为纪念这一历史性事件,欧洲临床研究基础网络(ECRIN)联合美国和加拿大,提议将每年的5月20日定为“国际临床试验日”,以此纪念临床试验鼻祖苏格兰海军军医詹姆斯·林德(James Lind)。在2005年5月20日,WHO在布鲁塞尔举行了第一个“国际临床试验日”。
二、什么是临床试验?
是指以人体(患者或健康受试者)为对象的试验,意在发现或验证某种试验药物的临床医学、药理学以及其他药效学作用、不良反应,或者试验药物的吸收、分布、代谢和排泄,以确定药物的疗效与安全性的系统性试验。
临床试验是一项长期医学研究过程中的最后阶段,目的是确定一种新药或一项治疗方法的疗效与安全性以及存在的副作用。未上市的药物虽然在动物身上已经进行了试验(临床前研究),但鉴于人和动物的差异,还需在人体(患者或健康受试者)做进一步的试验确认其安全性和有效性,从而找到预防、诊断和治疗疾病的最佳方案。
可依的;药物的疗效和安全性设计也往往是科学、严谨的。而规范的药物临床试验基本原则则可以在一定程度上保护患者。
药物临床试验主要遵循三大基本原则如下
1. 伦理道德原则:依据《赫尔辛基宣言》,此宣言也是所有临床试验需要遵守的第一原则,在任何时候保护受试者的安全和权益都是临床试验的首要条件。
2. 科学性原则:临床试验依据临床前试验资料,试验方案设计科学、观察指标和疗效判断、安全性评价科学,符合统计学原则。
3. 法规原则:临床试验应符合药物临床试验质量管理规范(GCP)和现行的相关管理法规。
我们开展的任何一项临床试验都必须基于《中华人民共和国药品管理法》《药品注册管理办法》《药物临床试验质量管理规范》等国家法律法规的要求,当药物在动物试验研究取得成功后,通过国家药品监督管理局及独立的伦理委员会审核批准,符合临床试验规范并取得批准文件后才可进入临床试验阶段。只有当试验药物被证实对患者确实安全有效后,才能够获得国家药品监督管理局的批准上市。
什么是临试验?
临床试验的临床试验的起源起源